Datos de los estudios clínicos de Jivi®: de 7 a <12 años
SEGURIDAD Y EFICACIA DEMOSTRADAS CON JIVI
Diseño de los estudios para niños de 7 a menos de 12 años
PROTECT Kids
Ensayo multicéntrico, prospectivo y de grupo único para evaluar la farmacocinética, la seguridad y la eficacia de Jivi para la profilaxis y el tratamiento del sangrado en niños menores de 12 años con hemofilia A grave que recibieron tratamiento previo (n = 73)1.
Alfa-PROTECT
Estudio multicéntrico, prospectivo y de grupo único para evaluar la seguridad de infusiones de Jivi para la profilaxis y el tratamiento del sangrado en niños de 7 a menos de 12 años con hemofilia A grave que recibieron tratamiento previo (n = 35)1.
Los datos de PROTECT Kids y Alfa-PROTECT se combinaron, ya que los dos estudios incluyeron a participantes de 7 a menos de 12 años. Los estudios se diseñaron para describir la seguridad y la eficacia clínica de Jivi en participantes de 7 a menos de 12 años con hemofilia A grave que recibieron tratamiento previo1.
Características del conjunto de análisis agrupado1
Pacientes que recibieron tratamiento previo (de 7 a menos de 12 años)*
57*
Duración del tratamiento (período de eficacia principal)
26 semanas
Grupo de análisis de eficacia principal
42 (profilaxis dos veces por semana)†
* La eficacia del tratamiento profiláctico se evaluó en 57 pacientes de 7 a menos de 12 años en los estudios PROTECT Kids y Alfa-PROTECT.
† 15 pacientes recibían tratamiento en un régimen de intervalos extendidos (cada 5 días o cada 7 días) en PROTECT Kids, por lo que no están incluidos en los datos de eficacia.
SEGURIDAD Y EFICACIA DEMOSTRADAS CON JIVI
Datos de seguridad para niños de 7 a menos de 12 años
Un producto de factor VIII con un perfil de seguridad demostrado
Las reacciones adversas más frecuentes (incidencia de ≥5%) en los ensayos clínicos en pacientes de ≥7 años tratados previamente (PTP) fueron dolor de cabeza, fiebre, tos y dolor abdominal1.
- No hubo eventos adversos graves relacionados con el fármaco del estudio2.
- Todos los eventos relacionados con el fármaco fueron leves o moderados2.
- EA relacionados con el fármaco: 6.7% (n = 4)2.
- Se produjeron cero inhibidores del FVIII2.
Un paciente pediátrico desarrolló anticuerpos contra el PEG, un componente de Jivi, lo que causó que Jivi no actuara adecuadamente y que se interrumpiera su tratamiento. El paciente reinició el tratamiento con Jivi 2 meses después de que los anticuerpos desaparecieron1.
- Tres pacientes pediátricos tuvieron anticuerpos temporales contra el PEG y, en dos de ellos, los niveles del factor estaban levemente reducidos. La recuperación del tercer paciente fue poco clara1.
SEGURIDAD Y EFICACIA DEMOSTRADAS CON JIVI
Frecuencia de dosificación e intervalo de los estudios
En el grupo combinado de PROTECT Kids y Alfa-PROTECT, la frecuencia de dosificación fue de dos veces por semana1.
Niños (de 7 a menos de 12 años)1* (N = 42)
Dosificación aprobada de Jivi para niños de 7 a menos de 12 años: El régimen posológico inicial recomendado de Jivi es de 60 UI/kg dos veces por semana. La dosis del paciente debe ajustarse según la respuesta clínica y/o la recuperación1.
* Pacientes agrupados de PROTECT Kids y Alfa-PROTECT de 7 a menos de 12 años, con un período de tratamiento de al menos 3 meses; población con intención de tratar (IDT) modificada.
PROTECCIÓN EFICAZ DE LAS HEMORRAGIAS CON JIVI
Tasas anualizadas de hemorragias (TAH)*
En los estudios PROTECT Kids y Alfa-PROTECT, las TAH para las hemorragias tratadas se evaluaron con respecto a Jivi en pacientes de 7 a menos de 12 años. La mediana de la TAH para las hemorragias totales, hemorragias articulares, hemorragias espontáneas y hemorragias por traumatismos fue de cero2.
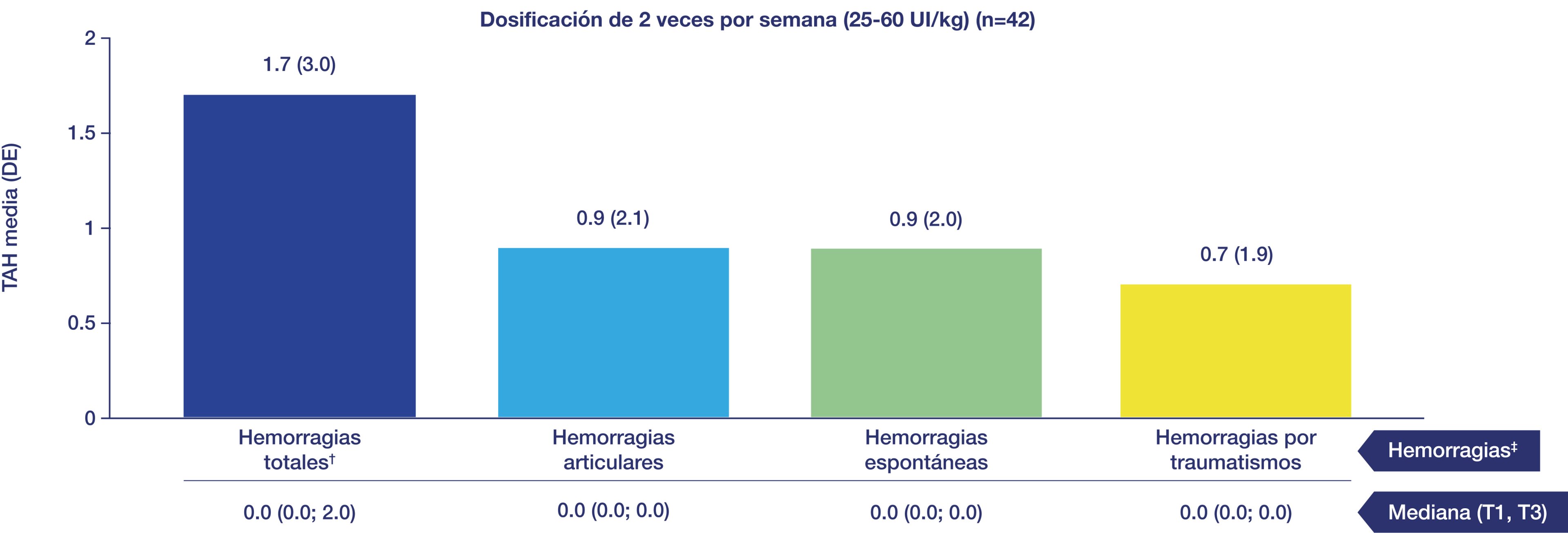
* La población con IDT modificada incluyó pacientes con un período de tratamiento de al menos 3 meses.
†El total de hemorragias incluye las hemorragias espontáneas, las hemorragias por traumatismos y las hemorragias articulares.
‡ Pacientes agrupados de PROTECT Kids y Alfa-PROTECT de 7 a menos de 12 años, población con IDT modificada.
PROTECCIÓN EFICAZ DE LAS HEMORRAGIAS CON JIVI
Porcentaje de pacientes con cero hemorragias
El porcentaje de pacientes con cero hemorragias durante el período del estudio completo de 26 semanas fue del 67%1. Dada la variación en la fecha de inicio del tratamiento de los pacientes y la duración exacta de la fase del estudio, los datos de tasas de cero hemorragias divididos por tipo de hemorragia se presentan para las últimas 24 semanas del período del estudio de 26 semanas.
En los estudios PROTECT Kids y Alfa-PROTECT, la mayoría de los pacientes presentaron cero hemorragias tratadas, incluidas las hemorragias espontáneas, las hemorragias articulares, las hemorragias por traumatismos y las hemorragias de articulaciones blanco2.
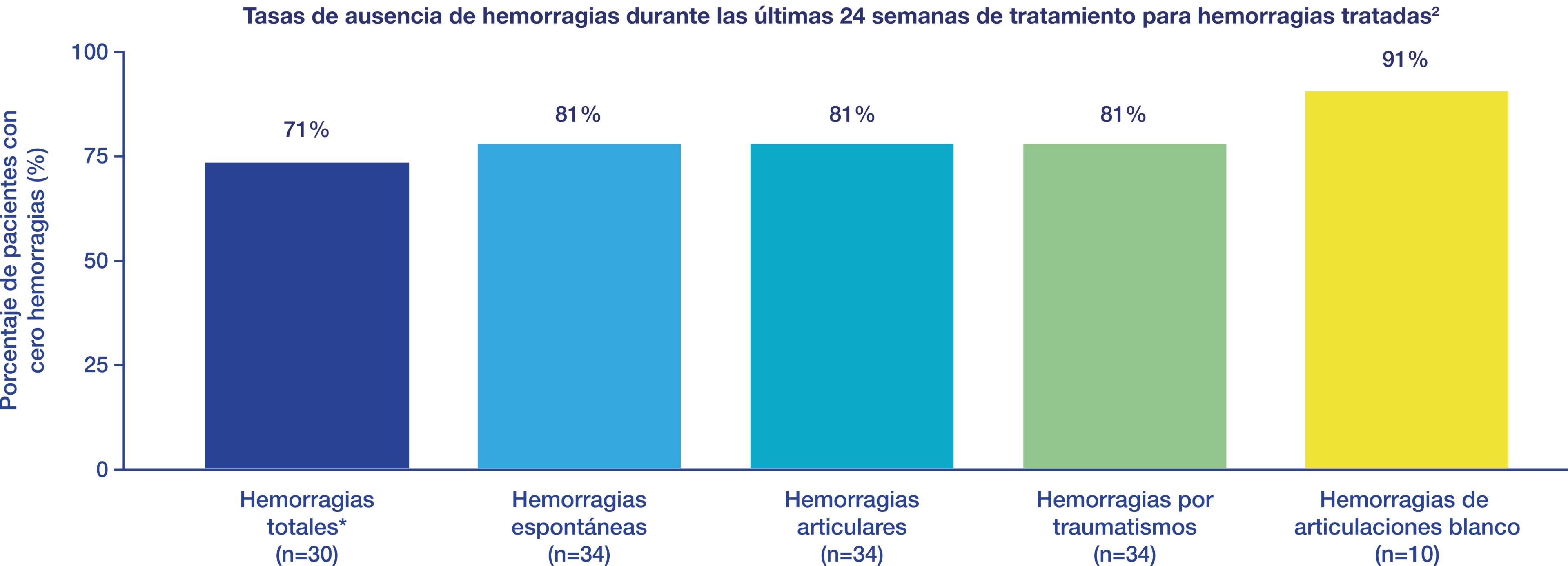
* El total de hemorragias incluye las hemorragias espontáneas, las hemorragias por traumatismos y las hemorragias articulares.
TRATAMIENTO EFICAZ DE LAS HEMORRAGIAS CON JIVI
Control de sangrado
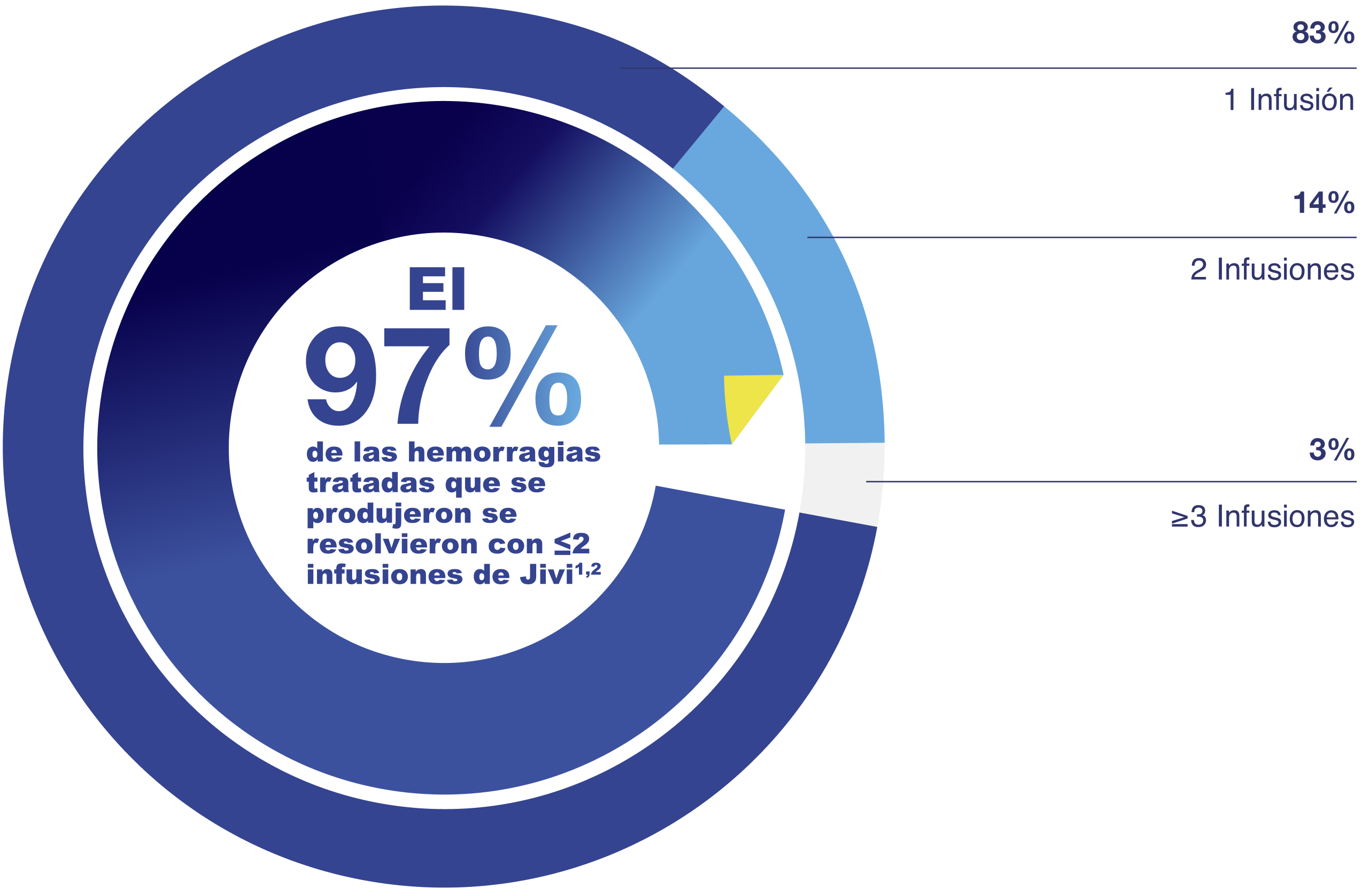
En los estudios PROTECT Kids y Alfa-PROTECT, un total de 36 episodios de hemorragias se trataron con Jivi en la población de 7 a menos de 12 años. El 97% de las hemorragias se trataron exitosamente con una o dos infusiones. La media (DE, desviación estándar) del tiempo de seguimiento entre infusiones fue de un (0.8) día1,2.
FARMACOCINÉTICA (FC)
Comprender la FC
¿Qué es la FC?
La FC describe cómo el organismo absorbe, distribuye, metaboliza y elimina un fármaco. Estas mediciones ayudan a determinar la dosificación del fármaco y la duración de la acción.
Términos de farmacocinética
- Área bajo la curva (ABC): La cantidad total de factor que es absorbida y distribuida en su torrente sanguíneo durante un período.
- Concentración máxima (Cmáx): La cantidad más alta de un fármaco en la sangre medida después de una dosis. Para un tratamiento con FVIII, esto a veces se denomina nivel de FVIII y se mide en unidades internacionales por decilitro (UI/dL).
- Vida media (t1/2): La cantidad de tiempo que tardan los niveles de factor en reducirse a la mitad (al 50%) de lo que eran originalmente justo después de su infusión.
- Depuración (CL): La velocidad a la que el factor se elimina de su organismo.
- Recuperación: El aumento estimado de factor VIII en la sangre poco tiempo después de una infusión de tratamiento de FVIII.
FARMACOCINÉTICA (FC)
Parámetros FC de Jivi
Ensayo cromogénico1 60 UI/kg

Los resultados se expresan como un valor promedio conocido como media aritmética.
ABC: área bajo la curva.
Cmáx: concentración máxima plasmática del fármaco después de una dosis.
t½: vida media terminal.
CL: depuración.
* n=131.
† n=141.
‡ Datos obtenidos de las muestras de recuperación de todos los pacientes, menos los que presentaron anticuerpos antifármaco, en un esquema de dos veces por semana (n=42) con un intervalo de 1.1-3.8 kg/dL1.
JIVI, ACOMPAÑANDO EN EL CRECIMIENTO
Dosificación en adultos y niños
Dosificación para niños de 7 a menos de 12 años

Dosificación gradual única para pacientes mayores de 12 años

INDICACIONES
JIVI es un medicamento inyectable que se utiliza para reemplazar el factor de coagulación (Factor VIII o factor antihemofílico) que no poseen las personas que padecen hemofilia A.
JIVI se utiliza para tratar y controlar las hemorragias en adultos y niños, a partir de los de 7 años de edad, con hemofilia A que recibieron tratamiento previamente. Su proveedor de atención médica también puede administrarle JIVI cuando se somete a una cirugía. JIVI puede reducir la cantidad de episodios de hemorragia en adultos y niños, a partir de los de 7 años de edad, con hemofilia A si se usa de manera regular (profilaxis).
JIVI no está indicado para usar en niños menores de 7 años o en pacientes que no recibieron tratamiento previo.
JIVI no está indicado para tratar la enfermedad de von Willebrand.
INFORMACIÓN DE SEGURIDAD IMPORTANTE
No debe utilizar JIVI si es alérgico a los roedores (como los ratones y hámsteres) o a cualquier ingrediente de JIVI.
JIVI puede provocar reacciones alérgicas. Llame a su proveedor de atención médica de inmediato e interrumpa el tratamiento si presenta opresión en el pecho o la garganta, mareos, disminución en la presión arterial o náusea. Es posible que ocurran reacciones alérgicas al polietilenglicol (PEG), un componente de JIVI.
Su cuerpo también puede fabricar anticuerpos, denominados “inhibidores”, contra JIVI o ciertos componentes de JIVI, como el polietilenglicol (PEG), lo que puede interrumpir la acción adecuada de JIVI. Consulte con su proveedor de atención médica para asegurarse de que será supervisado atentamente mediante análisis de sangre para detectar el desarrollo de inhibidores del Factor VIII. Informe a su proveedor de atención médica si le han informado que tiene inhibidores del Factor VIII.
Si su hemorragia no es controlada con su dosis habitual de JIVI, consulte con su médico de inmediato. Puede haber desarrollado inhibidores del Factor VIII o anticuerpos contra el PEG y su médico puede realizar pruebas para confirmarlo.
Los efectos secundarios frecuentes de JIVI son dolor de cabeza, fiebre, tos y dolor abdominal.
Estos no constituyen todos los posibles efectos secundarios de JIVI. Informe a su proveedor de atención médica acerca de cualquier efecto secundario que le moleste o no desaparezca.
Informe a su proveedor de atención médica sobre todas las enfermedades y/o condiciones médicas que tiene o que tuvo.
Para obtener información adicional importante sobre riesgos y uso, consulte la Información para Prescribir completa.
Referencias: 1. Jivi Prescribing Information. May 2025. Bayer. 2. Data on file. Whippany, NJ: Bayer; 2024. Clinical Study Report B003163.





